Het therapeutisch venster
De effectiviteit van parkinsonmedicatie is in hoge mate afhankelijk van de wijze waarop deze is ingesteld. Het loont dan ook zeker de moeite hier eens een keer bij stil te staan. Door te experimenteren met de inname frequentie kun je met dezelfde hoeveelheid medicijn een veel betere werking krijgen. Waarom krijg je bijvoorbeeld een recept van drie maal daags vijf tabletten. Waarom niet alles ineens, of vijf maal daags 3 tabletten, of welke andere combinatie dan ook. Het is duidelijk dat in het eerste geval de bijverschijnselen de pan uit zullen rijzen, terwijl al na een paar uren de therapeutische effecten zullen zijn verdwenen. Een te grote spreiding is weer heel onpraktisch omdat je dan de hele dag met medicijnen bezig bent, ongeveer zoals een verslaafde roker met zijn nicotine. Ik nodig hierbij de lezers van deze site van harte uit persoonlijke ervaringen met medicatie en eventuele bijwerkingen daarvan op dit forum te posten.
Ik neem aan dat het mogelijk is een optimum te vinden in de spreiding van medicatie, uitgaande van wat je waarneemt aan signalen van je eigen lichaam. Zo treden de bijverschijnselen meestal een half uur tot een uur na inname op. Daarna wordt het geleidelijk minder tot ze uiteindelijk helemaal verdwenen zijn. Door een ander inname schema te hanteren zou je van de bijverschijnselen af kunnen komen, of ze in ieder geval een stuk minder te maken.
 Figuur 1 Therapeutisch venster
Figuur 1 Therapeutisch venster
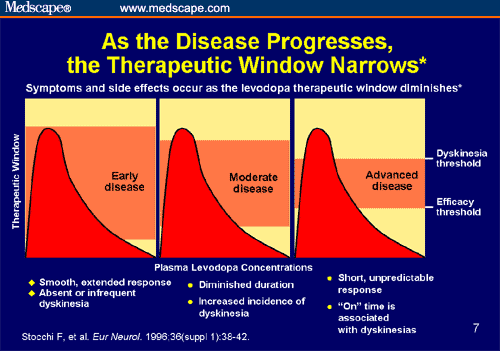
Het patroon waarin medicijnen als levodopa en agonisten in ons bloed worden opgenomen wordt geďllustreerd door bovenstaande figuur van Silver en Steward. Aanvankelijk stijgt het plasmaniveau snel, waarna de afbraak op gang komt en het niveau eerst snel en vervolgens steeds trager weg ebt. Als het niveau boven het oranje gebied komt, krijgen de bijverschijnselen de bovenhand; met name de dyskinesieën of onwillekeurige bewegingen. Komt het niveau onder het oranje gebied, dan is er sprake van een tekort met de daarbij horende parkinson verschijnselen. Het oranje gebied noemen zij het "Therapeutic Window", een therapeutisch venster waar je bij de behandeling van de Ziekte van Parkinson binnen zou moeten blijven.
In de loop van de ziekte schuift de ondergrens van dit venster naar boven met als gevolg dat je meer medicijn nodig hebt om de parkinson verschijnselen te bestrijden. Bovendien schuift de bovengrens naar beneden met als gevolg dat dyskiesiën al bij een lager plasmaniveau gaan optreden ("Dyskinesia threshold”). Om binnen het therapeutisch venster te blijven is één van de mogelijkheden de dosis te spreiden over de dag. Silver en Steward zeggen hierover: "We can fractionate the dose of levodopa, and probably there's a trend now to be using levodopa more frequently. Four times, 5 times, even 6 times a day. It's more of an inconvenience, but it can be done. So the goal is to reduce end-dose failure or off time by this fractionation, and you go from 3-4 doses, maybe 4-5 doses."
Hoe spreid je de medicatie?
Omdat hij niet vertelt hoe je dat spreiden zo goed mogelijk doet, en ik ook in de literatuur geen optimalisatieprocedure kan vinden, ben ik zelf aan de slag gegaan.
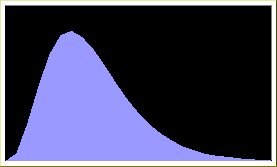
Door middel van "curve-fitting" ben ik gekomen tot de functie f(x)=a*b^x*x^c . Hiervoor heb ik het programma "Datafit" van Oakdale engineering gebruikt. Hiermee is de basiscurve gedefinieerd, die hieronder is afgebeeld. Vervolgens heb ik op www.drugs.com de gegevens over "half-life" (de tijd tussen de maximale plasmawaarde en het moment dat deze gehalveerd is) en "Tmax" (de tijd tussen het innemen van het medicijn en het moment dat de plasmawaarde maximaal is) van Requip ingevuld.
 Figuur 2 Basiscurve
Figuur 2 Basiscurve
Met behulp van de veronderstelde basiscurve (het blijft een gok) heb ik drie verdelingen doorgerekend:
- Dosering drie maal daags 5 tabletten van 1 mg met 5 uur tussenruimte. Het schema: 3 x (5 mg - 5 uur). De witte grafiek illustreert dit schema.
- Dosering drie maal daags 3 tabletten van 1 mg voor de maaltijd, en 2 tabletten 1 uur na de maaltijd. Het schema is dan dus 3 x (3mg - 1,5 uur - 2mg - 3,5 uur). De gele grafiek illustreert dit schema.
- Dosering 6 maal daags volgens het schema 3 x (3mg - 2,5 uur - 2mg - 2,5 uur). De rode grafiek illustreert dit schema.
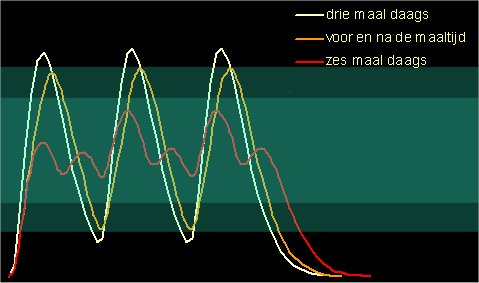 Figuur 3 Berekende plasmaniveau’s bij verschillende opnamefrequenties van de dopamine agonist Requip © 2005 j.oele
Figuur 3 Berekende plasmaniveau’s bij verschillende opnamefrequenties van de dopamine agonist Requip © 2005 j.oele
Achter de grafieken is het therapeutisch venster weergegeven in groen. In mijn geval wordt de bovenkant van dit venster niet bepaald door de dyskinesiën maar door andere bijverschijnselen, zoals plotseling verhoogd libido en slaapaanvallen. Ik heb de doseringen van de witte en de gele grafiek beide gedurende enkele weken opgevolgd. Toen ik overschakelde van het witte naar het gele schema merkte ik dat zowel de vermoeidheids-aanvallen als de periodes van verhoogd libido weg bleven. Om die reden is de bovengrens van het venster bepaald tussen de twee toppen in. Hetzelfde geldt voor de periodes van onvoldoende medicatie. Die zijn ook veel minder geworden ten opzichte van het witte doseringsschema, vandaar dat ook de onderkant van het venster tussen de witte en de zwarte dalen is komen te liggen.
 Figuur 4 Ongebufferd systeem
Figuur 4 Ongebufferd systeem
Buffering
De beschikbaarheid van dopamine in het lichaam is gebufferd. Bufferen is een cybernetisch mechanisme dat ervoor zorgt dat een wisselende input wordt omgezet in een constante output. Buffers kom je overal in de natuur tegen, en zijn vooral in de scheikunde een veel gehanteerd concept. In figuur 4 is te zien wat ik met een ongebufferd systeem bedoel. Hier is een opstelling getekend die een stroom met een bepaalde stof moet leveren (Het straaltje dat uit het gaatje komt). Als het vloeistofniveau tot het gaatje is gezakt, dat houdt de stroom echter op. Door de vloeistof weer bij te vullen, gaat de stroom weer lopen . Als dan ten slotte het gaatje weer wordt bereikt, stopt de stroom weer. Als het zo zou zijn geregeld met het dopaminerge systeem in het lichaam, dan zouden we regelmatig “off” zijn.
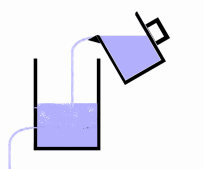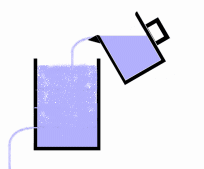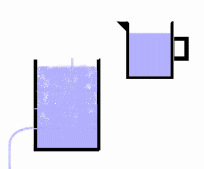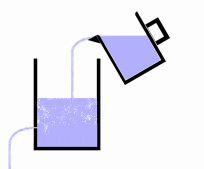 Figuur 5 Gebufferd systeem
Figuur 5 Gebufferd systeem
Door het vloeistof niveau iets hoger bij te vullen ontstaat een buffer waardoor de stroom niet wordt onderbroken. Voorwaarde is wel dat er voldoende vaak wordt bijgevuld, zodat de buffer in stand blijft. Het is daar waar het met de ziekte van Parkinson uiteindelijk mis gaat. Het systeem is niet in staat de buffer op tijd aan te vullen en de patiënt krijgt de symptomen van de ziekte. Door medicijnen te nemen wordt het bufferniveau weer hersteld, en verdwijnen de klachten. Het lichaam heeft echter een feedbackmechanisme waardoor de aanmaak van dopamine wordt gereguleerd. Daardoor loopt het vat niet over, en wordt ook weer op tijd nieuwe dopamine aangemaakt. Bij de toediening van medicijnen ligt dat natuurlijk wat gecompliceerder, onder andere om de volgende redenen:
- het lichaam is niet gestopt met produceren. - Het feedbackmechanisme is gelegen in de waarnemingen van de patiënt en erg onbetrouwbaar. - Het feedbackmechanisme wordt overruled door het doktersvoorschrift.
Om de medicatie goed in te stellen is het naar mijn mening eerst noodzakelijk het equilibrium punt vast te stellen. Dit is het punt waarbij de medicatie zodanig is dat de patiënt nog net “off” raakt. Dit moet heel traag gebeuren omdat in de fysieke toestand zoveel fluctuaties zitten dat je bij een snel opvoeren dat punt ongezien zou passeren. Als het equilibrium-punt is bereikt moet de patiënt een on-off patroon hebben dat met de medicatie op en neer gaat. Vervolgens moet de medicatie worden verhoogd zodanig dat de off-periodes geheel zijn verdwenen. Ook dat moet weer langzaam gebeuren vanwege de fluctuaties in de fysiek van de patiënt, maar ook omdat de buffer langzamerhand steeds voller wordt doordat het lichaam, met de extra hulp in de vorm van medicatie, het tempo weer kan bijbenen. De dopamine producerende cellen zelf vormen de bufferruimte. Als er te weinig van deze cellen over zijn, dan wordt op een gegeven moment de buffercapaciteit te klein. Als je niet oppast loopt het vat dan over. Ik kan me voorstellen dat dit in verband staat met de oorzaak van dyskinesieën. Silver en Steward vermelden dan ook dat de “Dyskinesia threshold” met name optreedt als de buffer te klein is geworden. Tegelijkertijd zal het vat in deze omstandigheid toch weer snel leeg zijn. In deze omstandigheid is het dus niet mogelijk de medicatie te verhogen. Wat dan nog overblijft is het aantal inname momenten te verhogen en de inname zelf te verkleinen.
De zandsloot
Een nadeel van het verkleinen is dat bij een verkleinde inname een relatief groot deel van de levodopa wordt afgebroken voordat het de blood-brain barričre kan passeren. Je zou het kunnen vergelijken met het dilemma van de boer die een stuk grond achter in zijn land wilde bevloeien. Hij groef een geul in het zand en goot daar water in. Het water drong echter in de grond voordat het het achterste land bereikte. Pas door de hoeveelheid water sterk te vergroten bereikte het water zijn achterste tuin. Het nadeel was wel dat zijn voorste tuin oververzadigd was met water met de daarbij horende nadelige gevolgen. Het is natuurlijk maar een beeld en het is niet duidelijk in hoeverre het ontstaan van diskinesieën verklaard kan worden door dopamine dat ontstaat door levodopa afbraak voordat het de blood-brain barričre is gepasseerd. Het model kan ook worden nagebouwd in een computergesimuleerd neuraal netwerk. Dat geeft een aantal verrassende suggesties, zoals het gedurende een korte periode toedienen van een grote hoeveelheid levodopa. Er gaat dan relatief weinig verloren terwijl de buffer toch wordt gevuld. Afwachten of dit in de praktijk zou kunnen werken, want er gaat toch veel verloren hetgeen toch tot bijwerkingen zou kunnen leiden.
Referenties:
Management of Levodopa Therapy in Parkinson's Disease (Live Web Conference) CME
Presenters: Dee E. Silver, MD and R. Malcolm Stewart, MD
Release Date: March 31, 2004; Valid for credit through March 31, 2005